Teplotní rozpínavost vzduchu určil francouzský fyzik Jacques Charles už v roce 1787 nezávisle na Louisi Gay-Lussacovi a Johnu Daltonovi, avšak veřejnost se o jeho výsledcích dozvěděla až na základě Gay-Lussacova článku, proto bývá tento zákon někdy také označován jako Gay-Lussacův izochorický zákon.
Jestliže v nádobě zajistíme konstantní objem, pak se daný děj nazývá izochorický, tzn. že platí V1 = V2. Pak stavovou rovnici dostaneme ve tvaru
![]()
neboli
![]()
Při izochorickém ději s ideálním plynem stálé hmotnosti je tlak plynu přímoúměrný jeho termodynamické teplotě. Grafickým znázorněním závislosti tlaku plynu na jeho termodynamické teplotě při izochorickém ději se nazývá izochora.
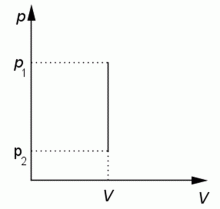
Grafická závislost tlaku na objemu.
Zdroj: Techmania Science Center. Autor: Magda Králová. Under Creative Commons.
Jak dokázal James Joule, vnitřní energie částic při izochorickém ději závisí pouze na teplotě. Při zvýšení teploty plynu o hodnotu ΔT přijme plyn teplo. Protože při izochorickém ději je objem plynu stálý, plyn nekoná práci. Z prvního termodynamického zákona plyne, že teplo přijaté ideálním plynem při izochorickém ději se rovná přírůstku jeho vnitřní energie.
Tento jev se vyskytuje např. při hoření paliva v zážehových spalovacích motorech, když je píst v úvrati.

